1.要 約
1.1 物質の同定、物理的・化学的特性、分析方法
1,2-ジクロロエタン(二塩化エチレン)は、室温では無色の合成化学物質である。また、揮発性が高く蒸気圧は8.5kPa(20℃)、水溶解性で、8,690mg/lの溶解度(20℃)を有する。Logオクタノール/水の分配係数は1.76である。
環境媒体中の1,2-ジクロロエタンは、通常、電子捕獲かフレームイオン化検出、もしくは質量分析と組み合わせてガスクロマトグラフィーにより分析される。検出限界の範囲は、空気中で0.016〜>4μg/m3、水中で0.001〜4.7μg/l、各種食品中で6〜10μg/kgである。
a 物質の同定
| 化学式 |
C2H4Cl2 |
| 化学構造 |
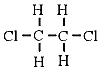 3次元 3次元 |
| 分子量 |
98.96 |
| 一般名 |
1,2-dichloroethane |
| その他の名称 |
EDC;1,2-DCE;1,2-bichloroethane;1,2-ethylene dichloride;acethylenchlorid;alpha, beta-dichloro-
ethane;bichlorure d'ethylene;ethylene dichloride;
ethylene chloride;glycol dichloride;sym-dichloro-ethane |
| 商品名 |
Borer sol, Brocide, Destruxo, 1Di-chlor-mulson,
Dichlor-mulsion, Dutch liquid, Dutch oil, ENT1656,
Freon150, Gaze Olefiant, Granosan(四塩化炭素も含有する) |
| CAS登録番号 |
107-06-2 |
| 換算係数 (25℃,760mmHg) |
1ppm=4mg/m3 |
| 1mg/m3=0.25ppm |
b 物理的・化学的特性
表 1,2-ジクロロエタンの物理的・化学的特性a
| 物理的状態 (常温) |
無色透明液体 |
| 臭気 |
クロロホルム様の甘い匂い |
| 密度 (20℃) |
1.253 |
| 沸点 (1atm) |
83℃ |
| 融点 (1atm) |
-35℃ |
| 蒸気圧 (20℃) |
8.5kPa |
| 水溶解性 (20℃) |
8,690mg/l |
n-オクタノール/水分配係数
(log Kow) |
1.76 |
| log Koc |
1.28 |
| ヘンリー定数 (25℃) |
111.5Pam3/mol |
| 引火点 |
12〜15℃ 揮発性、引火性が高い |
| 空気中引火限界 |
275〜700mg/l |
| 空気中飽和濃度 (20℃) |
350g/m3 |
| (30℃) |
537g/m3 |
| 赤外線吸収 |
波長7μm,12μm,13μm |
| 屈折率(rD20) |
1.4449 |
a Archer(1979);Chiou et al.(1979);Konemann(1981);
Warner et al.(1987);Worthing & Hance(1991)より
1.2 ヒトおよび環境の暴露源
1,2-ジクロロエタンの主要用途は塩化ビニルの合成であり、少量は各種の塩素化溶剤の製造に用いられる。また、ガソリンのアンチノック添加剤(一部の国においては、加鉛ガソリンの段階的使用禁止にともない、その使用は減少しているが)、燻蒸剤としても用いられてきた。1,2-ジクロロエタンの年間生産量は、1990年のカナダにおいては922キロトン(1キロトンはTNT火薬1,000トンの爆発力)、1991年の米国では6,318キロトンであった。
1.3 環境中の移動、分布、変質
環境中に放出される1,2-ジクロロエタンの大部分は、大気への排出である。それは大気中では中程度の持続性を示し、大気中での概算寿命は43〜111日の間であった。1,2-ジクロロエタンは成層圏に運ばれ、光分解により順次オゾンに変化する塩素ラジカルを生成することがある。1,2-ジクロロエタンの一部は工場廃水により水生環境内に放出され、その後、蒸発により速やかに除去される。1,2-ジクロロエタンは、産業廃棄物処理場近くの地下水にも浸出する。水生あるいは陸生生物種における生物濃縮はない、と考えられる。
1.4 環境中濃度とヒトの暴露
発生源に支配されていない地域の都市における近年の測定では、1,2-ジクロロエタンの平均濃度は0.07〜0.28μg/m3の範囲であったのに対し、住宅の室内空気中の平均濃度は<0.1〜3.4μg/m3の範囲が報告されている。飲料水中では、平均濃度は一般に0.5μg/m3以下である。1,2-ジクロロエタンは生物濃縮の可能性は低いため、最近の調査では食品中からはごくまれにしか検出されず、食品は主要な暴露源ではないようである。
各種の媒体からの平均暴露の推定に基づいた場合、一般集団への1,2-ジクロロエタンの主要な暴露源は屋内および屋外空気であり、ごく少量が飲料水による寄与である。食品からの1,2-ジクロロエタンの摂取は無視できるであろう。環境空気中からの吸入量は、産業発生源の周辺ではより多いであろう。
1.5 実験動物における体内動態と代謝
1,2-ジクロロエタンは、吸入、経口摂取、経皮暴露後に容易に吸収され、速やかに広く体内全般に分布する。ラットおよびマウスにおいては、速やかに、広範に代謝され、主として硫黄含有の代謝生成物として、用量依存的に尿中に排出される。ラットでは、5〜10μg/mlの血中濃度を生じさせる暴露濃度においては、代謝は飽和あるいは限定されるように見える。DNAのアルキル化は、6時間の吸入の場合よりも、塊(bolus)の強制投与による暴露の方が高いレベルを示した。
1,2-ジクロロエタンは、二種類の主な経路により代謝されるように見える。その第一の経路は、チトクロームP-450により、飽和ミクロソームに酸化され2-クロロアセトアルデヒドと2-クロロエタノールになり、次いでグルタチオンに抱合される経路を含む。第二の経路は、直接グルタチオンに抱合されてS-(2-クロロエチル)-グルタチオンを生成する。これは非酵素的にグルタチオン・エピスルホニウム・イオンに変換する。このイオンはDNA付加物を生成することがある。DNA損傷はin vitro(試験管内)においてP-450経路により誘発されるが、いくつかの証拠は、DNA損傷の主要経路として、グルタチオン抱合経路はP-450経路よりもおそらく重要であることを示している。
1.6 実験動物およびin vitro(試験管内)試験系への影響
実験動物における1,2-ジクロロエタンの急性毒性は低い。例えば、ラットに対する6および7.25時間の吸入LC50(50%致死濃度)は4,000〜6,600mg/m3、ラット、マウス、イヌ、ウサギの経口LD50は413〜2,500mg/kg体重の範囲であった。
数種類の実験動物における短期および亜慢性実験の結果は、肝臓と腎臓が標的臓器であることを示している。信頼できるNOELs(無影響量)あるいはLOELs(最小影響量)は、不適切な考証と、少数の動物において検討された限定的な範囲のエンドポイントのため、一般には設定されていない。初期における一連の限られた研究では、800mg/m3の気中濃度への亜慢性暴露後に、数種の動物において肝臓の形態学的変化が認められた。ラットに13週間、49〜82mg/kg体重/日以上を亜慢性経口投与したとき、肝臓の相対重量の増加が観察された。入手し得る慢性実験では、非腫瘍性の影響についての情報はほとんど得られない。202mg/m3の気中濃度に12カ月間暴露されたラットにおいては、肝臓と腎臓の毒性を示す血清パラメータの変化が認められたが、本研究では組織病理学的検索は行われなかった。
1,2-ジクロロエタンの発がん性は、実験動物による少数の限られた生物試験において検討された(短い暴露期間と高い死亡率が限界となっているが)。Sprague-Dawley系ラットまたはスイス系マウスに対して607mg/m3で78週間暴露させ、自然に死亡するまで観察した結果では、すべての種類の腫瘍の発生率の有意の増加は報告されていない。本研究におけるラットの死亡率は高かった。ただし、それは濃度との関連性は示さず、各群の間の異なる死亡率に対する発生率の調節はしなかった。200mg/m3で2年間暴露させたメスのSprague-Dawley系ラットでは乳腺腫と線維腺腫の有意ではない増加が見られた。この試験系では、化合物に関係するその他の毒性は観察されなかった。
以上とは対照的に、2種の動物における経口摂取後の腫瘍発生率について、有力な証拠が存在する。時間荷重平均連日投与量(TWA daily dose)で47あるいは95mg/kg体重/日を78週間強制経口投与したOsborne-Mendel系ラットのいくつかの部位において、腫瘍発生率の有意の増加[胃の扁平上皮がん(オス)、血管肉腫(オス・メス)、皮下組織の線維腫(オス)、乳腺の腺腫および線維腺腫(メス)を含む]が観察された。B6C3F1系マウスの複数部位における腫瘍発生率の同様の増加[肺胞/細気管支腺腫(オス・メス)、乳腺腺がん(メス)、子宮内膜間質ポリープあるいは子宮内膜間質複合肉腫(メス)]が、時間荷重平均連日投与量の97あるいは195mg/kg体重/日(オス)、また、149あるいは299mg/kg体重/日(メス)の78週間の強制経口投与により発生した。
1,2-ジクロロエタンの440〜594日間の皮膚反復塗布後には、メス・マウスにおいて肺腫瘍(良性の乳頭腫)の発生率が有意に増加した。1,2-ジクロロエタンの腹膜内への反復注射は、感受性の高い系統のマウスにおいて、一匹当りの肺腺腫数が用量関連的に増加したが、これらの増加はいずれも統計学的に有意ではなかった。1,2-ジクロロエタンの吸入と食餌中のジスルフィラムとの同時暴露は、ラットで肝臓内の胆管腫と嚢腫、皮下の線維腫、肝臓の腫瘍性の結節、精巣内の間質細胞腫瘍、乳腺がんの発生率は、いずれかの化合物のみを投与した動物あるいは投与のない対照群よりも増加を示した。これらの研究における組織病理学的検索の範囲は限られているが、3件の生物学的試験においては、腫瘍形成の誘発あるいは促進の可能性のないことは明らかであった。
In vitro試験において、1,2-ジクロロエタンはサルモネラチフィムリウム(Salmonella typhimurium)による変異原性試験では一貫して陽性を示した。その反応は、外因性活性系(チトクローム系による活性のためであろう)の存在下では、それを欠く場合よりも大きく、ヒトのGSTA1-1遺伝子を表現するサルモネラチフィムリウム(Salmonella typhimurium)においては、変異原性は2倍以上となった。哺乳類の培養細胞においては、1,2-ジクロロエタンはDNAと付加物を形成する。また、齧歯類およびヒトの一次培養細胞における不定期DNA合成と、数種の細胞系における遺伝子突然変異をも誘発する。ヒトの細胞系における変異原性の頻度は、グルタチオン-S-転移酵素活性の差異に関連を示した。In vivo研究においては、1,2-ジクロロエタンはキイロショウジョウバエ(Drosophia melanogaster)において体細胞および伴性劣性致死変異原性を、また、ラットおよびマウスにおけるすべての研究においてDNA結合化合物を誘発した。マウスを用いた研究では、肝臓において最初のDNA損傷と姉妹染色分体交換が認められたが、小核誘発の証拠はなかった。
少数の研究結果では、1,2-ジクロロエタンは実験動物に催奇形性を示す証拠は存在しない。また、他の全身影響を発生させる用量以下において、生殖および発生への影響を誘発するとの説得力のある証拠もほとんどない。1,2-ジクロロエタンの免疫毒性について入手し得るデータは限られている。
1.7 ヒトへの影響
1,2-ジクロロエタンの吸入あるいは摂取による急性の偶発的暴露は、ヒトにおいて、中枢神経系、肝臓、腎臓、肺、心臓血管系に種々の影響を与える。
1,2-ジクロロエタンに暴露された一般集団における発がんの可能性については、広くは研究されていない。主として1,2-ジクロロエタンに暴露された(他の化学物質との複合で)化学物質生産工場の作業者群において、膵臓がんによる死亡が有意に増加し、死亡率は暴露期間にともない増加を示した。さらに、例数は少なく、暴露期間との関連性については一貫性は低いが、これらの作業者の白血病による死亡も増加した。小規模の症例対照研究では、1,2-ジクロロエタンの職業暴露と脳のがんとの関連性は認められなかった。固有の限界を有する生態学的研究では、結腸および直腸がんの発生率は、飲料水中の1,2-ジクロロエタンの濃度とともに上昇したが、他の物質との同時暴露がこの影響に寄与している可能性がある。
1.8 実験室および自然界の標的以外の生物類への影響
実験室および自然界の多数の他の生物類に対する1,2-ジクロロエタンの暴露影響が検討されている。水生微生物類について、種々の影響に対するIC50(50%阻止濃度)あるいはEC50(50%効果濃度)は25〜770mg/lの範囲が報告されている。ミジンコ(Daphnia)に対するLC50(50%致死濃度)の最小報告値は220mg/lであるが、生殖の成功と成長に対する影響はそれぞれ20.7と71.7mg/lで認められた。入手し得るデータでは、最も感受性の高い淡水脊椎動物はノースウエスターン種のイモリ(Ambistoma gracile)と見られ、9日齢の幼生(孵化後4日)の生存は2.54mg/lにおいて減少した。陸生生物類に対する1,2-ジクロロエタンの毒性データの入手はごく限られている。
2.結論およびヒトの健康と環境の保護に対する勧告
1,2-ジクロロエタンの定性的・定量的双方の毒性学的特性を考慮すると、ヒトに対してどの経路でも悪影響を生じさせない暴露を推測することはできない。したがって、1,2-ジクロロエタンへのヒトの暴露を除去あるいは最小にするためのすべての適切な方法をとるべきである。
3.今後の研究
1,2-ジクロロエタンについての特定の研究は勧告されないが、追加的な分析疫学研究の実施が望ましい。
4.国際機関によるこれまでの評価
国際がん研究機関は、実験動物に対する発がん性の十分な証拠に基づいて、1,2-ジクロロエタンをグループ2B(ヒトに対して発がん性を示す可能性のある物質)(possiblycarcinogenic to humans)に分類した(IARC,1979)。
国際化学物質安全性計画(IPCS)は、以前に、1,2-ジクロロエタンの評価を行った(IPCS,1987)。その結論は、1,2-ジクロロエタンは中枢神経系の抑制と胃腸および肝臓の異常を発生させる、というものであった。実験動物でも、腎臓の異常、肺水腫、心臓血管系の機能不全の可能性のほかに同様の影響が認められた。1,2-ジクロロエタンの強制投与では、ラットおよびマウスにおいて発がん性を示し、実際的な目的のためには、ヒトに対して発がんのリスクをもたらす、と見なすべきである。1,2-ジクロロエタンは環境中において蓄積するとは考えられない。大気中においては、それはヒドロキシラジカルを経て光化学分解により除去され、水からは蒸発により排出される。オクタノール/水分配係数は低く、生物蓄積はないと考えられる。また、水生環境への危険は、事故や不適切な廃棄の場合以外はもたらされないと見られる。1,2-ジクロロエタンの陸生環境に対する影響を評価するには、データが不十分である。
国連食糧農業機関/世界保健機関の食品添加物専門家合同委員会(JECFA)は、3回にわたり1,2-ジクロロエタンの評価を実施した(FAO/WHO,1971,1980,1992)。最終評価において、委員会は「本物質はin vitroおよびin vivo試験系の双方において遺伝毒性を有し、経口経路による投与ではマウスおよびラットで発がん性を示す」との結論を下した。そのため、ADI(一日摂取許容量)は設定されなかった。委員会は、1,2-ジクロロエタンは食品中には使用すべきではない、との意見を表明した。
WHOの飲料水質ガイドライン(WHO,1993)では、米国立がん研究所の研究(1978)におけるオス・ラットの血管肉腫の発生率の線型多段階モデルに基づいて、10-4、10-5、10-6の過剰リスク(excess risk)に関連する飲料水中の1,2-ジクロロエタン濃度は、それぞれ300、30、3μg/m3であると予測した。
欧州委員会は、1990年、各種の工場のタイプごとの1,2-ジクロロエタンの排出限界値を定めた指令を公布した。これらの限界値は、金属のグリース除去に1,2-ジクロロエタンを使用する工場の0.1mg/l(月平均)から、1,2-ジクロロエタンを生産したり、加工・使用する工場に対する12mg/l(日平均)の範囲内である(CEC,1990)。
|
|